Клинико-морфологические особенности
дегенеративных изменений костной ткани
с остеопорозом в возрастных аспектах
Павлова Т.В., Башук И.П.
ФГАОУ ВО «Белгородский государственный национальный исследовательский университет»,
НИУ «БелГУ», г. Белгород
Актуальность. Наиболее часто встречающейся метаболической патологией скелета является остеопороз (ОП). Это системное заболевание характеризуется прогрессирующим снижением костной массы в единице объема кости по отношению к нормальному показателю у лиц соответствующего пола и возраста, нарушением микроархитектоники костной ткани, что приводит к повышенной хрупкости костей и увеличению риска их переломов от минимальной травмы и даже без таковой. После 50 лет каждая 3-я женщина и каждый 12-й мужчина страдают остеопорозом.
По данным Всемирной организации здравоохранения (2010), остеопороз считается третьей по частоте причиной смертности среди населения в возрасте старше 60 лет и уступает лишь заболеваниям сердечно-сосудистой системы и злокачественным новообразованиям [1, 2]. Переломы костей, особенно повторные, на фоне низкой минеральной плотности костной ткани (МПКТ) – важный диагностический признак остеопороза. Они часто приводят больных к стойкой инвалидности и существенно повышают уровень смертности [3, 4]. Так, пятилетняя летальность среди пациентов с остеопоротическими переломами бедренной кости или тел позвонков на 20% выше, чем у людей той же возрастной группы без переломов [3, 4].
При этом переломы бедренной кости являются причиной смерти у 3% людей среднего возраста, а от 15 до 30 % лиц пожилого возраста умирают после этих переломов в течение первого года после их получения. Остеопоротические переломы имеют ряд особенностей. Как следствие, они обычно возникают при минимальной нагрузке (падение с высоты, не превышающей собственный рост, неловкое движение) или даже без видимой причины. Наиболее характерными для остеопороза являются переломы проксимального отдела бедренной кости (шейки бедренной кости); дистального отдела костей предплечья и тел позвонков, хотя при значительном снижении минеральной плотности костной ткани могут отмечаться переломы любой другой локализации. В связи с неуклонным старением населения количество остеопоротических переломов неуклонно возрастает в среднем на 6,5% в год, что и определяет социальную значимость остеопороза и его последствий [1 – 4].
В современной диагностике остеопороза большое значение имеет морфометричекий метод. При этом решающее значение имеет не определение минеральной плотности костей (МПК), а выявление полостей в трабекулярных костях, через которые и происходят переломы. На основании этого В.И. Струков и соавторы полагают, что лечить остеопороз необходимо с закрытия полостей. Фирмой “Парафарм” и ГОУ ДПО ПИУВ разработаны новые технологии в лечении остеопороза – с использованием гормонов трутневого расплода (патент №2412616). В 1 таблетке Остеомед Форте содержатся витамин D3 – 500 МЕ/сут, труневый расплод – 100 мг, цитрат кальция – 500 мг. Необходимость ведения в препарат трутневого расплода объясняется тем, что он является донатором синтеза собственных половых гормонов (эстрадиола, прогестерона, тестостерона), оказывающих стимулирующее действие на восстановление метаболических полостных процессов и минеральную плотность костной ткани. Важное значение имеет динамическое наблюдение за размерами полостей при лечении остеопороза. При использовании Остеомед Форте, в комплексной терапии остеопороза был получен хороший лечебный эффект с уменьшением и закрытием полстей у 75% наблюдаемых пациентов [5 – 7].
Под термином «полость» (полостные образования) мы понимаем участки кости, где уже нет трабекул, костных клеток. Фактически в этом участке кости уже нет! Минеральная плотность в этом участке не костная, а мышечная. МПК дальше не снижается! Этот участок кости уже не имеет костной плотности, поэтому через такую полость и происходят переломы. Если не лечить остеопороз, то полость в размерах увеличивается и риск перелома возрастает [8 – 11].
Диагностика полостей имеет важное, практическое значение для выявления высокого риска переломов костей, принятия неотложных мер по лечению остеопороза и профилактике переломов! Наилучший способ выявления полостей в трабекулярных костях является рентгенабсорбционный метод (Osteometr DTX-100). Остальные остеометры полости не “видят”, к ним необходима специальная компьютерная программа. Несмотря на важность лучевой диагностики выявления полостей, недостаток метода в том, что мы не видим процессы происходящие внутри полости. Поэтому большую роль в изучении сложных метаболических процессов имеют микроскопические и цитохимические исследования резецированных участков костей, например головки бедренной кости. К сожалению таких исследований крайне недостаточно.
Цель исследования. Провести параллели между клиническими и морфо-биохимическими аспектами костной ткани у пациентов с переломами костей и дегенеративными заболеваниями опорно-двигательного аппарата на фоне системного остеопороза
Материалы и методы исследования. В исследование было включено 117 человек: 46 человек среднего возраста, 46 человек пожилого, 21 человек старческого возраста и 4 возраста долгожителей.
Пациенты с переломами имели типичную локализацию повреждений, характерную для переломов на фоне системного остеопороза: проксимальный отдел бедренной кости (чрезвертельная, подвертельная области, шейка), диафиз бедренной кости, дистальные метаэпифизы костей предплечья, проксимальный отдел плечевой кости (хирургическая и анатомическая шейки), диафиз плечевой кости. Группа больных с дегенеративными заболеваниями опорно-двигательного аппарата была представлена пациентами с деформирующим артрозом тазобедренных суставов III ст., поступившими в отделение в плановом порядке. Системный остеопороз у данной группы больных был подтвержден на основании данных рентгенографии, а также денситометрии.
Пациентам с переломами проводилось консервативное лечение повреждений (гипсовая иммобилизация), а также оперативное лечение по показаниям (репозиция костных отломков с последующим металлостеосинтезом). Всем пациентам с деформирующим артрозом тазобедренных суставов было произведено тотальное цементное эндопротезированиие сустава.
Всего прооперировано 77 пациентов, из которых 35 пациентов были среднего возраста, 30 пациентов преклонного возраста, 10 пациентов старческого возраста и 2 долгожителя.
Во время операции тотального цементного эндопротезирования тазобедренного сустава было произведено взятие костных макропрепаратов из резецированной головки бедренной кости. Проведено макроскопическое описание. Срезы, окрашенные гематоксилином и эозином, изучали в световом микроскопе «Topic-T» Ceti-Т. Для электронной микроскопии пробы фиксировали в стандартном глутаровом фиксаторе, а затем фотографировали и проводили морфометрический анализ с использованием растрового микроскопа FE1 Quanta 200 3D с приставкой для элементного анализа (Na, Mg, Al, S, Fe, C, N, O, P, Ca).
Результаты исследования и обсуждение. Количество больных с изолированными и множественными переломами костей было больше в группах среднего (n=46; 30 женщин и 16 мужчин) и пожилого возраста (n=46; 38 женщин и 8 мужчин). Однако, отмечалось снижение количества пациентов со скелетной травмой в группах пожилого возраста и долгожителей. Данное явление можно объяснить снижением функциональной активности пациентов старческого возраста и долгожителей, а также с наличием таких гериатрических синдромов как дементные состояния, старческая астения, саркопения, падения, которые рассматриваются как один из компонентов синдрома старческой астении и возникают у 30 ±5% лиц старше 65 лет и у 40%±5% лиц старше 80 лет. Нарушения походки с замедлением скорости передвижения, неустойчивость в позе, укорочение шага являются компонентами старческой астении и часто способствуют падениям. Падения ухудшают функциональное состояние, мобильность, увеличивают риск повторных госпитализаций, они сопряжены с формированием тревожно-депрессивного состояния, страха повторных падений. Это также объясняет снижение количества пациентов с дегенеративными поражениями суставов в выше указанных группах. У большинства людей ± (65-100%) старше 60-ти лет имеется одно или несколько сопутствующих хронических заболеваний (сердечно-сосудистой, дыхательной систем, сахарный диабет, почечная патология). Было выявлено, что с возрастом происходило уменьшение количества больных, которым проводилось оперативное лечение в объеме металлостеосинтеза и эндопротезирования тазобедренного сустава, что объяснялось появлением противопоказаний к операции по мере декомпенсации хронических заболеваний. Снижение качества костной ткани, взятой интраоперационно, было подтверждено при исследовании микропрепаратов. При остеопорозе морфологически наблюдалось уменьшение общей площади костной ткани. В губчатом веществе костные пластинки истончались и перфорировались, а также, частично разрушаясь, сливались между собой, образуя крупные полости (Рис.1). Решетчатая система трабекул становилась более тонкой и частично прерывалась. Трабекулы, истончаясь, рассасывались, расстояния между ними увеличивалось. В губчатом веществе происходило истончение, однако под надкостницей сохранялось небольшое количество остеонов. Внутри кости микропереломы костных балочек сопровождались мелкими кровоизлияниями из которых формировались свертки (Рис. 1.А, 2). Выявлена остеогеная клеточно-волокнистая ткань (Рис. 2). Из нее формировалась микромозоль грубоволокнистого строения.
Рисунок 1. Фрагмент головки бедренной кости, полученной в результате операции тотального эндопротезирования тазобедренного сустава женщины 60 лет с диагнозом «закрытый трансцервикальный перелом бедренной кости на фоне системного остеопороза». В ткани – крупные полости неправильной формы, с неровными краями. В части из них (рис. А) – тромбы.
СЭМ. Рис. А (х100), рис. Б (200).
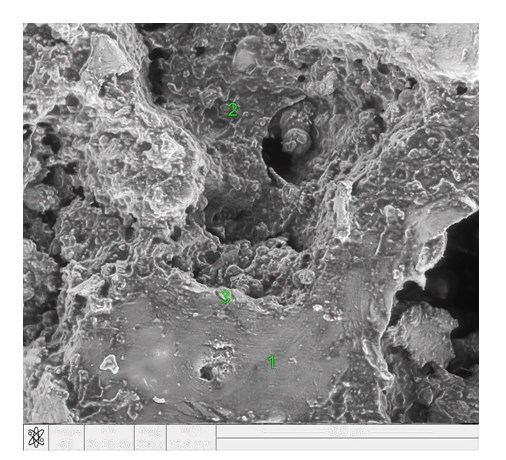
Рисунок 2. Фрагмент ткани тазобедренного сустава, полученного в результате операции тотального эндопротезирования тазобедренного сустава женщины 65 лет с диагнозом «закрытый субкапитальный перелом бедренной кости на фоне системного остеопороза».
В ткани – крупные полости неправильной формы (2), с неровными краями, а также грубоволокниствая фиброзная ткань (1).
СЭМ. (х200).
Таблица 1
Элементный состав костной ткани тазобедренного сустава больных среднего возраста 40-60 лет (0%)
| Участки с фиброзной тканью (участок 1) | Участки между фиброзной тканью и некротизированной (участок 3) | Участки некротизированной
ткани (участок 2) |
|
| C | 50.91±3.06 | 73.40±4.85* | 73.91±3.95* |
| N | 3.70±0.65 | 2.94±032 | 2.61±038 |
| O | 18.63±2.02 | 14.14±2.01* | 14.00±1.09* |
| Na | 0.27±0.03 | 0.10±0.02* | 0.09±0.01* |
| Mg | 0.20±0.05 | 0.10±0.02* | 0.08±0.01* |
| P | 8.00±1.56 | 3.03±0.37* | 2.7±0.28* |
| Ca | 18.29±2.01 | 7.29± 1.32* | 6.31±1.48* |
*р<0,05 ( в сравнении с фиброзной тканью)
При микроскопическом исследований костной ткани были выявлены участки с фиброзной тканью, участки некротизированной ткани, а также переходные участки между выше указанными зонами. При элементном анализе было выявлено достоверное снижение N (3.70±0.65, 2.61±038), O (18.63±2.02, 14.00±1.09, р<0,05), Na (0.27±0.03, 0.09±0.01, р<0,05), Mg (0.20±0.05, 0.08±0.01, р<0,05), P (8.00±1.56, 2.7±0.28, р<0,05), Ca (18.29±2.01, 6.31±1.48, р<0,05) в участка с некротизированной тканью, по сравнению с участкам с фиброзной тканью. При этом отмечалось увеличение C (50.91±3.06, 73.91±3.95, р<0,05) у участках с некротизированной тканью.
Таблица 2
Элементный состав костной ткани тазобедренного сустава больных преклонного возраста 60-75 лет
| Участки с фиброзной тканью (участок 1) | Участки между фиброзной тканью и некротизированной
(участок3) |
Участки некротизированной
ткани (участок2) |
|
| C | 52.90±4.31 | 70.50±4.22* | 70.93±3.45* |
| N | 3.81±0.75 | 2.94±0.32 | 2.60±0.38 |
| O | 16.63±3.45 | 12.18±2.65* | 12.20±2.43* |
| Na | 0.26±0.02 | 0.13±0.03 | 0.09±0.04 |
| Mg | 0.11±0.03 | 0.06±0.02 | 0.07±0.03 |
| P | 6.00±1.08 | 1.90±0.05* | 2.50±0.75* |
| Ca | 20.29±2.87 | 12.29± 1.68* | 11.31±2.01* |
*р<0,05
При элементном анализе было выявлено достоверное снижение N (3.81±0.75, 2.60±038), O (16.63±3.45, 12.20±2.43, р<0,05), Na (0.26±0.02, 0.09±0.04, р<0,05), Mg (0.11±0.03, 0.07±0.03, р<0,05), P (6.00±1.08, 2.50±0.75, р<0,05), Ca (20.29±2.87, 11.31±2.01, р<0,05) в участка с некротизированной тканью, по сравнению с участкам с фиброзной ткани. При этом отмечалось увеличение C (52.91±4.31, 70.93±3.45, р<0,05) у участках с некротизированной тканью.
При сравнении показателей элементного состава костной ткани больных среднего возраста 40-60 лет и больных преклонного возраста 60-75 лет было выявлена общая тенденция к увеличению показателей C, а также достоверное снижение показателей N, O, Na, Mg, P, Ca в участках с неротизированной тканью по сравнению с участками фиброзной ткани. При этом у пациентов преклонного возраста содержание выше указанных элементов было меньше, за исключением показателей уровня Na, содержание которого не изменилось.
Таким образом, нами была выявлена закономерность, согласно которой, по мере старения пациентов в костной ткани на фоне грубых морфологических изменений, связанных с прогрессированием остеопороза, происходят изменения на уровне микроэлементов, которые заключаются в постепенном снижении уровней содержания C, N, O, Na, Mg, P, Ca в участках с некротизированной тканью. Необходимо дальнейшее исследование о влиянии современных методов лечения остеопороза на морфологические изменения в костной трабекулярной ткани. Это важно для разработки более эффективных методов лечения остеопороза у пожилых людей.
Список использованной литературы
- Лесняк О.М. Фармакоэкономика средств профилактики и лечения остеопороза. В кн.: Руководство по остеопорозу. М., 2003. с. 469-481.
- Лесняк О.М., Торопцова Н.В., Евстигнеева Л.П. Остеопороз. Профилактика и амбулаторное ведение пациентов. Методические рекомендации. М., 2013.44с.
- Миронов С.П. Остеопороз как медико-социальная проблема. В кн.: Проблема остеопроза в травматологии. М.; 2006. с. 3.
- Рожинская Л.Я. и др. Результаты Российского многоцентрового исследования эффективности стронция ранелата у женщин с постменопаузальным остеопорозом. Остеопороз и остеопатии. 2007;(3):25-30.
- Струков В.И., Катюшина Ю.Г., Филиппова О.В. Остеомед – эффективный регулятор минеральной плотности костей и закрытия полостных образований при лечении пресенильного и сенильного остеопороза. Поликлиника. – 2013; 1 (1): 90–1.
- В.И. Струков, Д.Г. Елистратов. Известные и новые технологии в лечении и профилактике остеопороза. Методические рекомендации. Пенза, 2014. С.46.
- Strukov V.I. and othe «Method for fillingbone cavit formations with calcium». Патент Японии, Y88-10001-00, March 2.2016.
- Sambrook P., Cooper C. Osteoporosis. Lancet. 2006;367:2010-2018.
- Lekamwasam S, Adachi JD,. Agnusdei D et al. A framework for thedevelopment of guidelines for the management of glucocorticoid-inducedosteoporosis. 2012;23(9):2257-76
- Recommendations for the acute and long-term medical management of lowtrauma hip fractures. Cassim B et al. JEMDSA 2013 Volume 18 No 1
- Reducing mortality from hip fractures: a systematic quality improvement programme. Radcliffe Lisk et al. BMJ Quality Improvement Reports 2014; October. P 1-6