И. Сарвилина, доктор медицинских наук
Медицинский центр «Новомедицина», Ростов-на-Дону
Врач №5, 2016
Выявлена положительная динамика показателей активности псориатической артропатии (ПА), обусловленная молекулярными звеньями механизма действия препарата Остеомед Форте на фоне базисной терапии. Остеомед Форте перспективен в лечении активной ПА и ее профилактике и хорошо переносится.
Ключевые слова: псориатическая артропатия, лечение, профилактика, Остеомед Форте.
Р аспространенность псориаза в мире – от 1 до 3%. В США псориазом поражено 4,5 млн (2,1%) человек и еще 1 млн (0,5%) страдают псориатической артропатией (ПА). Распространенность псориаза минимальна среди китайцев (0,4%), в Западной Африке (0,3–0,7%) и среди афроамериканцев (0,7%). Среди японцев и индийцев его распространенность составляет соответственно 0,3–1,0 и 0,8%, в кавказской популяции варьирует от 1 до 5% (Farber Е., 1991), в Австралии приближается к 2,5% (Duffy D., 1993). В странах Западной Европы этот показатель распределился следующим образом: 3% – в Дании (Brandrup F., Green L., 1981), 4,8% – в Норвегии
(Kavli G., 1985). В России распространенность псориаза достигла 217,4 на 100 тыс. населения, ПА – 12,3 (5,7% всех случаев псориаза; у взрослых – 5,5%, у детей – 0,2%). Заболеваемость ПА в России – 1,8 на 100 тыс. населения (0,3 у детей и 2,1 у взрослых) [2].
Наблюдается бимодальное распределение заболеваемости в зависимости от возраста: 1-й пик приходится на 15–35 лет, 2-й – на 57–60 лет, у детей – на 10 лет [8]. У женщин средний возраст возникновения заболевания ниже, чем у мужчин. Псориаз ухудшает качество жизни (КЖ), причем ухудшение может сравниться с таковым при гипертензии, сахарном диабете, депрессии. Ежегодные расходы на лечение псориаза в США составляют 3 млрд долларов но эти затраты не улучшают КЖ пациентов. В исследовании М. Feldmann и соавт., в которое были включены 578 пациентов с псориазом, показано, что ежегодные затраты на ведение 1 пациента составляют 800 долларов [7]. В исследовании С. Ellis и соавт. пациенты получали терапию этретинатом, затраты на которую составили 2300 долларов в год (при других видах лечения затраты составили 10 000 долларов в год) [6].
Наиболее частым осложнением псориаза ПА является в возрасте от 30 до 50 лет. ПА характеризуется сочетанным поражением суставов конечностей и позвоночника и относится к серонегативным артритам. Предикторы неблагоприятного течения ПА – молодой возраст и мужской пол. Развитие ПА обусловлено взаимодействием генетических, иммунологических факторов и факторов внешней среды. Иммунологическая составляющая патогенеза проявляется клеточными инфильтратами в коже и ткани суставов, высокой экспрессией иммуноглобулинов в эпидермисе и синовиальной мембране. В сыворотке крови регистрируются повышение уровней IgА (у 90%) и IgG, циркулирующих иммунных комплексов, антител (АТ) к компонентам кожи и антинуклеарных АТ, снижение ответа Т-лимфоцитов, уменьшение супрессорной клеточной функции, экспрессия фактора некроза опухоли-α. Триггерами развития ПА являются бактериальная, вирусная и другие инфекции [1]. В патогенезе ПА ключевую роль играет нарушение кальциевого обмена. Перераспределение кальция приводит к перестройке нейроиммуноэндокринной регуляции и нарушению функций на субклеточном, клеточном, тканевом, органном и системном уровнях, в том числе в коже и суставах.
Данные клинических исследований позволяют рекомендовать для лечения обострения хронического псориаза и ПА циклоспорин, системные ретиноиды (ацитретин, этретинат), комбинацию синтетических аналогов витамина D3 (кальципотриол, такальцитол) с топическими стероидами, фумараты, нестероидные противовоспалительные препараты (НПВП). Данные, касающиеся применения метотрексата, гидреа, азатиоприна, сульфасалазина, хондропротекторов, неубедительны [3]. Новые терапевтические агенты (алефацепт, эфализумаб, этанерсепт, инфликсимаб, адалимумаб) характеризуются специфическим воздействием на молекулы-мишени, определяющие патофизиологические процессы при псориазе [9, 10]. Отсутствуют новые лекарства, регулирующие нейроиммуноэндокринные взаимодействия при ПА путем влияния на кальциевый обмен и связанные с ним молекулярные патологические пути. Один из важных этапов создания оригинальных лекарств – разработка, внедрение и анализ механизмов эффективности биологически активных добавок как источников новых молекул для создания эффективных средств терапии ПА.
Нашей задачей явилось исследование молекулярных механизмов эффективности при ПА препарата Остеомед Форте: цитрат кальция, биологически активная добавка гомогенат трутневый с витамином В6, пиридоксина гидрохлорид (витамин В6), витамин D3; вспомогательные вещества: лактоза, кальция стеарат (ООО «Парафарм», Россия) [4, 5].
Исследование являлось пострегистрационным, проспективным, с параллельным дизайном и проводилось в соответствии с «Правилами проведения качественных клинических испытаний – GCP)» (ОСТ №42-511-99 от 29.12.98), принципами Декларации Хельсинки /Токио /Венеция /Гонконг /Вашингтон /Эдинбург /Сеул (1964–2008).
В исследование включали мужчин и женщин в возрасте с 18 до 70 лет с диагнозом ПА в соответствии с CASPAR (CLASsification criteria for Psoriatic ARthritis, 2006) и модифицированными критериями Bennet и соавт.; с наличием не менее 5 болезненных и 5 припухших суставов; получавших стабильную дозу НПВП и топических глюкокортикостероидов на протяжении всего исследования и за 28 дней до начала лечения; не получавших базисной терапии в течение 28 дней до начала лечения; давших добровольное информированное согласие на участие в исследовании. Критерии невключения в исследование: атипичные формы или прогрессирующее течение вульгарного псориаза; отказ пациента от участия в программе клинического исследования; повышенная чувствительность к компонентам препарата Остеомед Форте; беременность, кормление грудью; тяжелые соматические заболевания, влияющие на течение ПА и иммунный статус; прием иммуномодуляторов и системных противовирусных средств, препаратов кальция, витамина D3 и В6 менее чем за 3 мес до момента включения в программу или во время участия в программе; наличие на момент включения в программу любого острого инфекционного заболевания; нарушение функции печени или почек; нарушение функции кроветворения, выявленное на скрининговом визите; наличие других артритов и артропатий; алкоголизм, наркомания; сопутствующая онкологическая патология.
В исследование было включено 60 пациентов с диагнозом ПА (М07, М07.00, М07.01, М07.3) в возрасте старше 18 лет согласно клинико-анамнестической характеристике, представленной в табл. 1. 40 пациентов были рандомизированы в 2 группы: пациенты 1-й группы (n=20) получали в период обострения ПА мелоксикам (15 мг/сут после еды, 1 мес), кальципотриол/бетаметазон (наружно, тонким слоем, 1 раз в сутки, 1 мес); пациенты 2-й группы (n=20) – мелоксикам (15 мг/сут после еды, 1 мес); кальципотриол/бетаметазон (наружно, тонким слоем, 1 раз в сутки, 1 мес); Остеомед Форте (по 2 таблетки 2 раза в день во время еды, 1 мес). Контрольную группу (КГ) составили 20 пациентов с ПА, не получавших лечения. Длительность исследования составила 6 мес; пациенты основных групп (n=40) в течение 5 мес продолжали терапию Остеомед Форте (по 2 таблетки 2 раза в день во время еды).
Таблица 1 Клинико-анамнестическая и лабораторная характеристика пациентов с ПА на момент начала исследования
| Показатель | 1-я группа (n=20) | 2-я группа (n=20) | КГ (n=20) |
| Анамнестические данные | |||
| Пол (мужчины/женщины) | 13/7 | 14/6 | 9/11 |
| Возраст, годы | 33,8±4,2 | 34,5±4,5` | 34,0±3,9 |
| Масса тела, кг | 76,7±5,1 | 77,0±5,3` | 75,9±5,2 |
| Рост, см | 168,2±5,0 | 170,2±5,2` | 171,3±5,5 |
| Длительность псориаза, годы | 12,5±1,3 | 11,9±1,1` | 12,1±1,2 |
| Длительность ПА, годы | 5,3±0,5 | 5,7±0,6` | 5,5±0,5 |
| Средняя частота рецидивов в год | 3,9±0,6 | 3,8±0,4` | 3,8±0,5 |
| Длительность рецидива, дни | 28,1±2,3 | 28,5±2,5` | 28,3±2,4 |
| Средняя продолжительность
межрецидивного периода, мес |
2,2±0,8 | 2,4±0,5` | 2,4±0,5 |
| Критерии ПА CASPAR, баллы | |||
| Псориаз:
на момент осмотра в анамнезе семейный анамнез псориаза |
2 0,5±0,2 0,5±0,2 |
2 0,5±0,3 0,5±0,3 |
2 0,5±0,2 0,5±0,2 |
| Псориатическая дистрофия ногтей:
точечные вдавления, онихолизис, гиперкератоз |
1 | 1 | 1 |
| Отрицательный ревматоидный фактор
(кроме метода латекс-теста) |
1 | 1 | 1 |
| Дактилит:
припухлость всего пальца в момент осмотра дактилит в анамнезе |
1 0,5±0,3 |
1 0,5±0,3 |
1 0,5±0,3 |
| Рентгенологические признаки внесуставной
костной пролиферации по типу краевых разрастаний (кроме остеофитов) на рентгенограммах кистей и стоп |
1 | 1 | 1 |
| Лабораторные синдромы | |||
| АЦЦП, Ед/мл | 2,2±0,5 | 2,2±0,5 | 2,2±0,5 |
| СОЭ, мм/ч | 27,7±2,9 | 27,2±2,8 | 25,5±2,6 |
| СРБ, мг/л | 21,8±1,6 | 22,2±1,9` | 21,5±1,5 |
| HLA B27-антиген, нет/есть | 13/7 | 15/5 | 20/0 |
| Активность ПА, баллы | |||
| Минимальная | 14 | 15 | 13 |
| Умеренная или высокая и при наличии факторов
неблагоприятного прогноза |
6 | 5 | 7 |
Для оценки клинической эффективности и безопасности стандартного и модифицированного режимов лечения ПА на момент начала исследования и через 6 мес терапии применялись следующие методы: анализ амбулаторных карт, истории болезни и жизни пациента; физикальные, инструментальные и лабораторные – ЭКГ («АТЕС МЕДИКА», Россия); эзофагогастродуоденоскопия (GIF-E3, Olympus, Corp., Япония); УЗИ органов брюшной полости, почек и надпочечников; эхокардиография; рентгенографическое исследование кистей, стоп, таза (в прямой проекции) и переходного отдела позвоночника (нижнегрудного с захватом поясничного в боковой проекции; SonoAce R3, Medison Samsung, Южная Корея); магнитно-резонансная томография суставов для ранней диагностики (Intera 1,5T, Philips, Нидерланды); общеклинический анализ крови (Advia 120, Bayer Diagnostics, Германия; Sysmex XT 2000i, Hoffman LaRoche, Швейцария) и мочи (CLINITEK Advantus Urine Analyzer, Siemens, США); биохимический анализ крови; исследование уровня железа, трансферрина, СРБ, альбумина и глобулиновых факторов, ревматоидного фактора сыворотки крови, липидограммы (Olympus AU640, Япония), АТ к циклическому цитруллинированному пептиду, уровней АТ в крови к хламидиям (иммунохимический анализатор ARCHITECT i2000, Abbott Laboratories, США); бактериологическое исследование крови на стерильность; коагулограмма (ACL-9000 и ACL ElitePro,
Instrumentation Laboratory, США); общеклинический анализ синовиальной жидкости; анализ на HLA B27-антиген (цитометр FC 500, Beckman Coulter, США).
Молекулярное фенотипирование синовиальной жидкости выполнялось на этапах процедуры очистки (аффинная хроматография с лектином, Amersham Biosciences; Sigma, St. Louis, MO), разделения на белковые фракции методом одномерного электрофореза в полиакриламидном геле (SDS-PAGE) с идентификацией белков и пептидов методом массспектрометрического анализа на основе MALDI-TOF-МС (прибор Autoflex III, Bruker, США). Применяли программное обеспечение для протеомики и масс-спектрометрии (Flex Control, Flex Analysis 2.x с функцией Auto Xecute, ClinProTools 1.0., Biotools 3.0.) и идентификацию пептидного фингерпринта молекулярных маркеров в интегрированной базе данных Mascot Search (v2.1, Matrix Science, Великобритания). Результаты представлены в виде молекулярного профиля синовиальной жидкости, включающего выявленные белки с указанием их молекулярной массы – Mr (Да). Условием для включения белка в диагностический профиль являлся показатель «покрытия сиквенса» при анализе (>15%) масс-спектрограмм. Биоинформационный анализ межмолекулярных взаимодействий белков синовиальной жидкости проведен на основе программы String 9.1.
Мониторинг безопасности терапии предусматривал оценку частоты, характера, выраженности, длительности неблагоприятных побочных реакций (НПР) и их связи с приемом препарата.
Для оценки активности ПА пациентом и врачом применялись показатели PsARC (Psoriatic Arthritis Response Criteria): число болезненных суставов (ЧБС) из 68; число припухших суставов (ЧПС) из 66); PASI/BSA (индексы тяжести и распространенности псориаза); оценка боли пациентом (ОБП) по визуальной аналоговой шкале (ВАШ); оценка активности заболевания пациентом (ОЗП) по ВАШ; HAQ (функциональный индекс КЖ). Для оценки выраженности боли использовали 5-балльную шкалу Likert. Критериями эффективности терапии являлись оценка пациентом и врачом течения заболевания: улучшение (уменьшение общей оценки активности ПА пациентом и врачом на ≥ 1 пункт; уменьшение ЧБС/ЧВС на ≥ 30%); ухудшение (увеличение общей оценки активности ПА пациентом и врачом на ≥ 1 пункт; увеличение ЧБС/ЧВС ≥ 30%).Оценка кожного синдрома производилась на момент начала исследования и через 6 мес терапии с помощью цифровой оценочной шкалы, пронумерованной от 0 до 10 (шкала зуда), общей оценки врачом активности псориаза по 5-балльной шкале Likert и PASI (Psoriasis Area and Severity Index). Влияние поражения кожи на повседневную деятельность пациентов определяли по опроснику DLQI (Dermatology Life Quality Index).
Для статистической обработки материала применяли пакет программ Statistica 12.0.
При включении в исследование выявлены пациенты с: преимущественным поражением дистальных межфаланговых суставов кистей и стоп (дистальная форма; n=18); асимметричным моноолигоартритом (n=25); симметричным полиартритом (ревматоидоподобная форма; n=17). Все пациенты полностью завершили курс лечения в соответствии с протоколом исследования.
Изменения ЧБС, ЧВС, уровня боли и активности ПА по ВАШ, оцененные больным и врачом, представлены в табл. 2. Показана высокая частота наступления эффекта при приеме терапии с включением Остеомед Форте: отмечено уменьшение ЧБС, ЧВС, уровня боли и активности ПА по ВАШ после 6 мес лечения; снижение ОЗП на 37%, оценки активности болезни врачом на 22% по сравнению с исходными значениями. Менее выраженные изменения отмечены в случаях применения стандартного режима терапии. При анализе динамики активности болезни по 5-балльной шкале Likert за период 6 мес отмечено значимое улучшение во 2-й группе по сравнению с 1-й. Выявлено выраженное уменьшение среднего значения индекса HAQ к концу 6-го месяца во 2-й группе по сравнению с 1-й: соответственно на 40,5 и 36,0%. У 18 (90%) пациентов 2-й группы к концу 6-го месяца модифицированной терапии достигнуто значимое уменьшение HAQ (в 1-й группе – у 8–40%). К концу лечения ответили на терапию в соответствии с PsARC 17% больных в 1-й группе и 31% – во 2-й при отсутствии изменений в КГ. Наиболее выраженное улучшение индекса PASI, показателей шкалы зуда и DLQI к моменту окончания лечения наблюдалось в 2-й группе. Статистически значимое уменьшение уровня СРБ отмечено к окончанию лечения в обеих основных группах по сравнению с таковым в КГ; выраженное снижение уровня СРБ отмечено во 2-й группе (пациенты, принимавшие дополнительно Остеомед Форте); см. табл. 2. НПР во время лечения препаратом Остеомед Форте не зарегистрированы.
Таблица 2 Оценка активности ПА и выраженности боли, динамика параметров кожных симптомов на фоне стандартной и модифицированной терапии
| Параметр | На момент начала исследования, % | Через 6 мес терапии, % | ||||
| КГ (n=20) | 1-я группа (n=20) | 2-я группа (n=20) | КГ (n=20) | 1-я группа (n=20) | 2-я группа (n=20) | |
| ЧБС | 18 | 16 | 17,5 | 18,5 | 12 | 8 |
| ЧВС | 14,5 | 12 | 13,5 | 15 | 8 | 5 |
| Боль по ВАШ, мм | 57 | 55,5 | 54,5 | 53 | 35 | 32 |
| Оценка активности заболевания
больным по ВАШ, мм |
63 | 61,5 | 62 | 61 | 45 | 35 |
| Оценка активности заболевания
врачом по ВАШ, мм |
59 | 55 | 57 | 57 | 39 | 35 |
| Оценка активности заболевания
по Likert больным, баллы |
3 | 3 | 3 | 3 | 2 | 1,5 |
| Оценка активности заболевания
по Likert врачом, баллы |
3 | 2,5 | 2,5 | 3 | 2,5 | 2 |
| HAQ | 1,55 | 1,47 | 1,43 | 1,53 | 0,94 | 0,85 |
| Параметры кожного синдрома | ||||||
| PASI | 8,6 | 9,2 | 8,8 | 8,8 | 6,8 | 5 |
| DLQI | 7,5 | 8,5 | 8,0 | 7,5 | 7,5 | 5,5 |
| Шкала зуда | 3 | 2,5 | 3 | 3 | 2,0 | 1,5 |
| Лабораторные параметры (M±SEM) | ||||||
| СОЭ, мм/ч | 28,5±1,7 | 26,4±1,6 | 26,5±1,5** | 27,8±1,6 | 25,3±1,5** | 25,9±1,3** |
| СРБ, мг/л | 22,4±1,4 | 21,6±1,2 | 22,5±1,5** | 22,0±1,1 | 15,4±0,8* | 8,7±0,3* |
Примечание. PASI – композитная оценка эритемы, инфильтрации, шелушения и площади псориатической бляшки; DLQI – шкала оценки влияния поражения кожи на повседневную деятельность пациентов; М – среднее значение; SEM – стандартная математическая ошибка; * – различия достоверны при p<0,001; ** – различия недостоверны.
Динамика молекулярных процессов, объясняющих изменения в суставах при ПА, представлена в табл. 3: на фоне приема базисной терапии и препарата Остеомед Форте зарегистрировано уменьшение экспрессии в синовиальной жидкости катепсина G, матриксной металлопротеиназы-1, миелопероксидазы, белка, связывающего галектин-3, CРБ, белка S100A9, стромелизина-1, нейтрофильного альфа-дефензина-1, CD5-подобного белка, α2-гликопротеина 1, содержащего лейцин, и увеличение экспрессии орозомукоида-1, профилина-1, гистона-4, ингибитора лейкоцитарной эластазы, пластина-2,C4b-связывающего белка по сравнению с КГ; менее выраженная динамика экспрессии белков-маркеров суставного синдрома наблюдалась в протеомном профиле синовиальной жидкости пациентов 1-й группы. Протеомная карта оригинального состава трутневого расплода в составе препарата Остеомед Форте позволила выполнить биоинформационный анализ межмолекулярных взаимодействий активных молекул белков и молекул белков синовиальной жидкости, что раскрывает механизм действия препарата.
Таблица 3 Динамика протеомного профиля синовиальной жидкости у пациентов с ПА на фоне приема стандартной и модифицированной терапии
| Название белка | Mr, Да | На момент начала исследования, % | Через 6 мес терапии, % | ||||
| КГ (n=20) | 1-я группа (n=20) | 2-я группа (n=20) | КГ (n=20) | 1-я группа (n=20) | 2-я группа (n=20) | ||
| Орозомукоид-1 | 23603 | 25 | 30 | 25 | 25 | 65 | 80 |
| Катепсин G | 28837 | 75 | 70 | 80 | 75 | 65 | 25 |
| Профилин-1 | 15054 | 40 | 65 | 60 | 45 | 70 | 90 |
| Гистон-4 | 11367 | 25 | 40 | 45 | 75 | 70 | 80 |
| Mатриксная металлопротеиназа-1 | 22000 | 100 | 90 | 90 | 100 | 80 | 25 |
| Ингибитор лейкоцитарной эластазы | 26073 | 35 | 35 | 30 | 35 | 60 | 70 |
| Миелопероксидаза | 83869 | 70 | 75 | 65 | 70 | 70 | 40 |
| Пластин-2 | 21792 | 35 | 30 | 30 | 35 | 60 | 75 |
| Галектин-3-связывающий белок | 65331 | 90 | 90 | 90 | 90 | 70 | 20 |
| C4b-связывающий белок | 67033 | 20 | 30 | 20 | 20 | 45 | 75 |
| CРБ | 25039 | 100 | 100 | 100 | 100 | 80 | 30 |
| Белок S100A9 | 13242 | 100 | 100 | 100 | 100 | 85 | 30 |
| Стромелизин-1 | 53977 | 90 | 90 | 95 | 90 | 70 | 25 |
| Нейтрофильный альфа-дефензин-1 | 10201 | 90 | 90 | 90 | 85 | 75 | 40 |
| CD5-подобный белок | 38088 | 75 | 70 | 75 | 75 | 65 | 45 |
| α2-гликопротеин-1, содержащий лейцин | 38178 | 60 | 65 | 65 | 60 | 45 | 25 |
Примечание. CD – кластер дифференцировки.
Рассмотрим молекулярные механизмы реализации эффектов препарата Остеомед Форте с учетом выявленной динамики протеомного профиля синовиальной жидкости на фоне терапии, а также знаний о протеомном составе трутневого расплода в препарате.
Идентифицированные белки синовиальной жидкости пораженного сустава относятся к 4 группам: белки острофазового сигнального ответа; белки гранулоцитарной адгезии и диапедеза; участники продукции окиси азота и свободнорадикального оксиления в макрофагах; белки межклеточной сигнализации и взаимодействия, клеточного цикла, антигенной презентации на поверхности клеток.
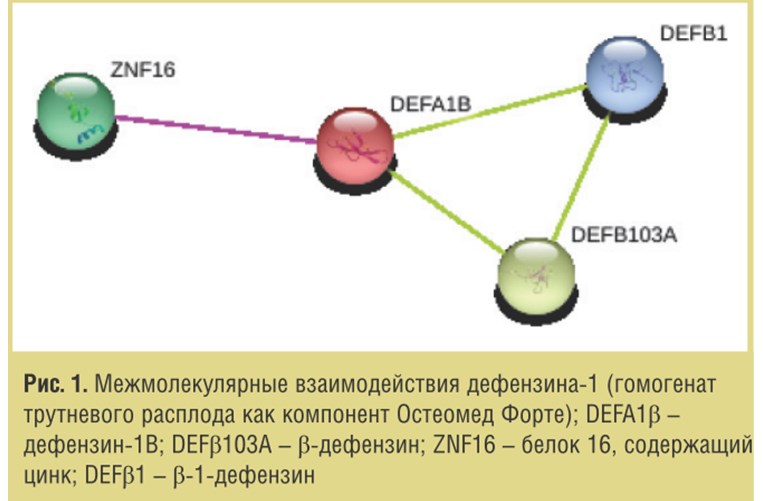
Альфа-дефензин-1 секретируется нейтрофилами в ответ на появление антигена. Его высокая экспрессия в синовиальной жидкости связана с воспалительной активностью при ПА. Альфа-дефензин-1 выполняет роль антимикробной защиты при синовиальном воспалении. Экспрессия альфадефензина-1 является хорошим индикатором прогрессирования ПА и эффективности средств его лечения. Дефензин-1 в трутневом расплоде в препарате «Остеомед форте» дает противомикробный эффект (рис. 1).
Увеличение экспрессии гем-содержащего фермента миелопероксидазы в синовиальной жидкости пациентов с ПА до приема терапии связано с активностью воспалительного процесса. Снижение активности данного белка в синовиальной жидкости, наиболее выраженное при модифицированной терапии, может быть связано с активностью дефензина-1 и лизоцима-2 в составе препарата Остеомед Форте.
Снижение экспрессии CD5-подобного белка на фоне базисной терапии и Остеомед Форте подтверждает наличие в молекулярном механизме действия последнего влияния на активированные при ПА Т-клетки, что делает данный маркер релевантным для оценки патологической активности клеточного иммунитета и выявления иммунотропного эффекта в спектре фармакодинамических эффектов средств лечения ПА.
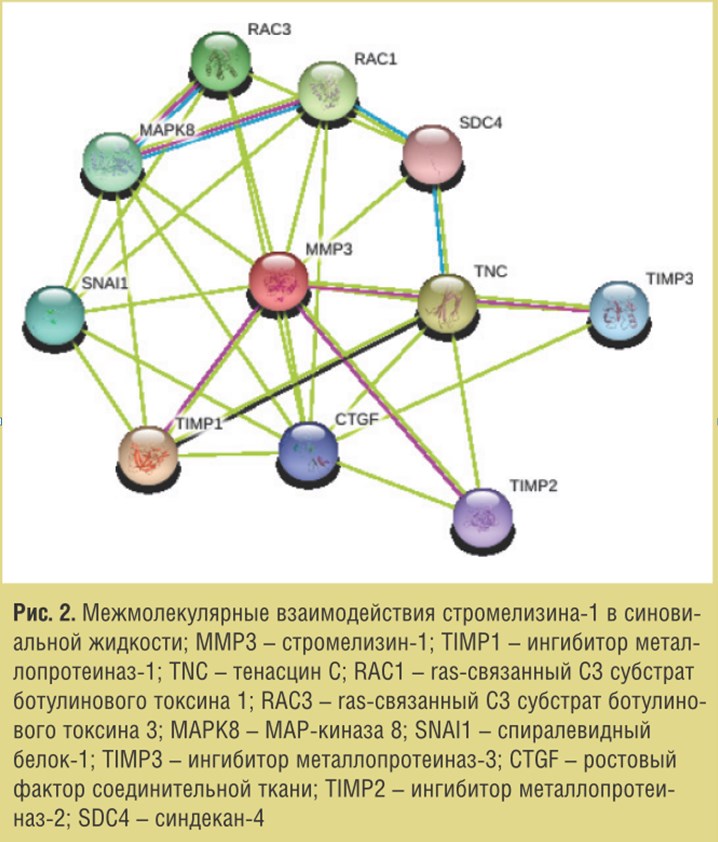
Значимое уменьшение экспрессии матриксной металлопротеиназы-1 в синовиальной жидкости сустава при приеме Остеомед Форте в режиме лечения ПА свидетельствует о снижении интенсивности патологического ремоделирования в суставных тканях благодаря защите от разрушения коллагена I, II и III типов. Снижение экспрессии стромелизина-1 в синовиальной жидкости при приеме модифицированной терапии ПА отражает уменьшение активности процессов деградации фибронектина, ламинина, желатинов I, III, IV и V типов, коллагена III, IV, IX и X типов, протеогликанов суставного хряща (рис. 2).
Уменьшение высокой экспрессии катепсина G в синовиальной жидкости, наиболее выраженное во 2-й группе, связано со снижением интенсивности ремоделирования соединительной ткани в участках воспаления. Снижение экспрессии катепсина G ассоциировано с увеличением экспрессии ингибитора лейкоцитарной эластазы в синовиальной жидкости при применении Остеомед Форте. Последняя уменьшает гибель клеток суставных тканей, индуцируемую катепсином G при ПА. Значимое уменьшение высокой экспрессии α2-гликопротеина-1, содержащего лейцин, во 2-й группе свидетельствует о снижении интенсивности воспалительного процесса и неоваскуляризации в суставных тканях, опосредованной фактором роста опухоли-β.
Снижение экспрессии белка S100A9 на фоне базисной терапии и терапии препаратом Остеомед Форте в синовиальной жидкости при ПА отражает устранение интенсивности воспаления, поддерживаемого в суставе неоваскуляризацией суставных тканей и привлечением лейкоцитов в очаг воспаления. Прием базисной терапии ПА и препарата Остеомед Форте сопровождался уменьшением экспрессии белка, связывающего галектин-3, в синовиальной жидкости. Данный факт свидетельствует о снижении выраженности иммунного ответа в суставных тканях, связанного с естественными киллерами и клеточной цитотоксичностью, во 2-й группе.
Увеличение экспрессии белка орозомукоида-1 в синовиальной жидкости на фоне приема модифицированного режима терапии отражает участие молекулы в иммуносупрессивном эффекте базисной терапии и препарата Остеомед Форте при ПА. Наибольшее увеличение экспрессии белка профилина-1 в синовиальной жидкости во 2-й группе свидетельствует об эффективном восстановлении процессов полимеризации актина в ответ на внеклеточные сигналы. Рост экспрессии гистона-4 в синовиальной жидкости в 1-й группе и в большей степени – во 2-й свидетельствует о стабилизации хроматинового материала в клетке и устранении эпигеномных перестроек при ПА на фоне терапии. Существенное увеличение экспрессии пластина-2 в синовиальной жидкости пораженного сустава при ПА в условиях базисного режима терапии и приема Остеомед Форте отражает реставрацию репликативной активности клеток тканей суставов. Увеличение экспрессии C4b-связывающего белка и уменьшение экспрессии СРБ в синовиальной жидкости пораженного сустава при ПА на фоне приема препарата Остеомед Форте способствует блокаде классического и лектин-ассоциированного пути комплемента в суставных тканях.
Представлены межмолекулярные взаимодействия витамина D3, содержащегося в препарате Остеомед Форте, механизм действия которого связан с активацией рецептора витамина D, индукцией транскрипционных факторов и рецепторов ядра. Конечный эффект витамина D3 – поддержание кальциевого гомеостаза при формировании костной ткани, в том числе контроль клеточного роста, дифференцировка и апоптоз, что делает перспективной данную молекулу в терапии ПА (рис. 3).
Исследование показало, что препарат Остеомед Форте оказывает отчетливое симптом-модифицирующее действие в отношении суставного синдрома у больных ПА, подтвержденное положительной динамикой результатов стандартных исследований и обусловленное молекулярными звеньями механизма действия препарата Остеомед Форте на фоне базисной терапии ПА.
Результаты исследования позволяют рассматривать Остеомед Форте как препарат, высокоэффективный в лечении активной ПА и обладающий хорошей переносимостью. Перспективы дальнейшего применения препарата в комплексной терапии ПА связаны с его потенциальными возможностями замедлять прогрессирование заболевания и уточнением его фармакодинамических эффектов.
Итак, исследование выявило высокую эффективность и безопасность приема препарата Остеомед Форте в составе стандартной терапии ПА; определены ключевые молекулярные звенья реализации фармакодинамических эффектов препарата Остеомед Форте у пациентов с ПА; продемонстрирована целесообразность дальнейшего поиска новых молекул-мишеней для разработки лекарственных средств лечения ПА.
Литература
- Галлямова Ю. А. Псориатическая артропатия // Лечащий врач. – 2008; 3: 28.
- Знаменская Л.Ф., Мелехина Л.Е., Богданова Е.В. и др. Заболеваемость и распространенность псориаза в Российской Федерации // Вестн. дерматол. и венерол. – 2012; 5: 20–9.
- Пирузян Л.А., Голденкова И.В., Корсунская И.М. и др. Экогенетические аспекты при создании протоколов ведения пациентов с псориазом // Проблемы стандартизации в здравоохранении. – 2006; 6: 7–14.
- Струков В.И. и др. Способ и препарат для профилактики и лечения атипичного остеопороза с нормальной или повышенной минерализацией костной ткани с наличием полостных образований в трабекулярных отделах костей (и ему близких состояниях при избыточной массе и метаболичнеском синдроме). Патент РФ на изобретение №2497533. Зарегистрирован
- 11.13 г.
- Струков В.И., Елистратов Д.Г., Максимова М.Н. и др. Способ диагностики остеопороза и определения эффективности препарата в лечении заболевания // Фармация. – 2013; 8: 40–3.
- Ellis , Hermann R., Gorsulowsky D. et al. Etretinate therapy reduces in patient treatment of psoriasis // J. Am. Acad. Dermatol. – 1987; 17: 787–91.
- Feldmann S., Garton R., Averrett W. et al. Strategy to manage the treatment of severe psoriasis: considerations of efficacy, safety and cost // Expert Pharmacother. – 2003; 4: 1525–33.
- Henseler T., Christophers E. Psoriasis of early and late onset: characterization of two types of psoriasis vulgaris // J. Am. Acad. Dermatol. – 1985; 13: 450–6.
- Mease P., Goffe B., Metz J. et al. Etanercept in the treatment of psoriatic arthritis and psoriasis: a randomised trial // Lancet. – 2000; 356 (9227): 385–90.
- Mease P., Ory P., Sharp J. et al. Adalimumab for long-term treatment of psoriatic arthritis: 2-year data from the Adalimumab Effectiveness in Psoriatic Arthritis Trial (ADEPT) // Ann. Rheum. – 2009; 68 (5): 702–9.
MOLECULAR MECHANISMS OF THE EFFICACY OF OSTEOMED FORTE IN PSORIATIC ARTHROPATHY
- Sarvilina, MD
«Novomeditsina» Medical Center, Rostov-on-Don
Positive changes have been found in the activity of psoriatic arthropathy (PA) caused by the molecular components of the mechanism of action of Osteomed Forte during basic therapy. The drug is promising in treating and preventing PA and well tolerated.
Key words: psoriatic arthropathy, treatment, prevention, Osteomed Forte.
Молекулярные механизмы эффективности препарата Остеомед Форте при псориатической артропатии